Page 18 - สถานภาพและการจัดการดินเปรี้ยวในประเทศไทย
P. 18
ห้องสมุดกรมพัฒนาที่ดิน
ปริมาณของอินทรียวัตถุที่สามารถย่อยสลายได้ง่ายและปริมาณเพียงพอ แร่เหล็กที่จะทำปฏิกิริยากับกำมะถันหรือ
ซัลไฟด์และเกิดเป็นสารประกอบไพไรต์ และมีสารประกอบซัลเฟตอย่างเพียงพอ โดยทั่วไป ในน้ำทะเลมี
สารประกอบซัลเฟตที่เพียงพอและไม่ก่อให้เกิดอุปสรรคในการเกิดไพไรต์อยู่แล้ว
2-
กระบวนการเกิดสารประกอบไพไรต์จะเริ่มจากสารประกอบซัลเฟต (SO4 ) จะถูกรีดิวซ์เป็น
ไฮโดรเจนซัลไฟด์ (H2S) โดยแบคทีเรียพวก Desulfovibrio และ Desulfotomaculum sp. ที่อยู่อย่างอิสระในน้ำ
ทะเลทั่วๆ ไป ดังสมการที่ (2.1) โดยอาศัยแหล่งคาร์บอนจากอินทรียวัตถุที่มาจากเศษซากพืช
SO4 + 2CH2O H2S + 2HCO3 (2.1)
2-
-
ไฮโดรเจนซัลไฟด์จะทำปฏิกิริยากับสารประกอบเหล็กซัลไฟด์ (FeS) เพื่อสร้างสารประกอบไพไรต์ (FeS2) กลไกอีก
2-
ประการหนึ่งของการเกิดไพไรต์คือปฏิกิริยาระหว่างโพลีซัลไฟด์ (Sx ) และ FeSaq โดย FeSaq เกิดขึ้นจากการแตก
ตัวของสารประกอบเหล็กซัลไฟด์ (FeS) โพลีซัลไฟด์อาจจะเกิดมาจากหลายปฏิกิริยา แต่ส่วนใหญ่ผ่านปฏิกิริยา
2-
0
ระหว่าง S และ S (ภาพที่ 2.1)
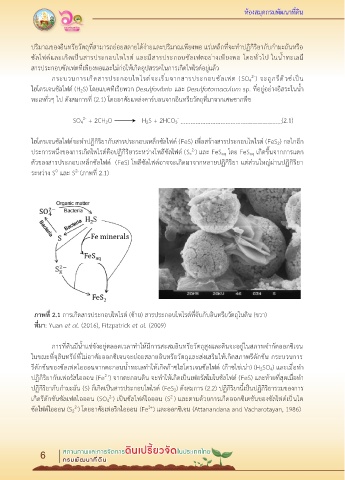
ภาพที่ 2.1 การเกิดสารประกอบไพไรต์ (ซ้าย) สารประกอบไพไรต์ที่จับกับอินทรียวัตถุในดิน (ขวา)
ที่มา: Yuan et al. (2016), Fitzpatrick et al. (2009)
การที่ดินมีน้ำแช่ขังอยู่ตลอดเวลาทำให้มีการสะสมอินทรียวัตถุสูงและดินจะอยู่ในสภาพจำกัดออกซิเจน
ในขณะที่จุลินทรีย์ที่ไม่อาศัยออกซิเจนจะย่อยสลายอินทรียวัตถุและส่งเสริมให้เกิดสภาพรีดักชัน กระบวนการ
รีดักชันของซัลเฟตไอออนจากตะกอนน้ำทะเลทำให้เกิดก๊าซไฮโดรเจนซัลไฟด์ (ก๊าซไข่เน่า) (H2SO4) และเมื่อทำ
2+
ปฏิกิริยากับเฟอรัสไอออน (Fe ) จากตะกอนดิน จะทำให้เกิดเป็นเฟอรัสโมโนซัลไฟด์ (FeS) และท้ายที่สุดเมื่อทำ
ปฏิกิริยากับกำมะถัน (S) ก็เกิดเป็นสารประกอบไพไรต์ (FeS2) ดังสมการ (2.2) ปฏิกิริยานี้เป็นปฏิกิริยารวมของการ
2-
เกิดรีดักชันซัลเฟตไอออน (SO4 ) เป็นซัลไฟด์ไอออน (S ) และตามด้วยการเกิดออกซิเดชันของซัลไฟด์เป็นได
2-
2-
ซัลไฟด์ไอออน (S2 ) โดยอาศัยเฟอริกไอออน (Fe ) และออกซิเจน (Attanandana and Vacharotayan, 1986)
3+
6 สถานภาพและการจัดการดินเปรี้ยวจัดในประเทศไทย
กรมพัฒนาที่ดิน