Page 32 - วิธีวิเคราะห์ไนเตรทอย่างง่ายในห้องปฏิบัติการด้วยน้ำยาสกัด Mehlich I
P. 32
ห้องสมุดกรมพัฒนาที่ดิน
25
2. การเตรียมกราฟสารละลายมาตรฐานไนเตรท
การเตรียมกราฟของสารละลายมาตรฐานไนเตรทจากสภาวะที่เหมาะสมในการเกิดปฏิกิริยา
ของการวิเคราะห์ไนเตรท ผลการศึกษา พบว่า ความสัมพันธ์ของสารละลายมาตรฐานไนเตรทความ
เข้มข้น 0 - 12.5 มิลลิกรัมต่อลิตร กับค่าการดูดกลืนแสงที่ได้ มีลักษณะเป็นเส้นตรง ให้ค่าสมการ
2
ถดถอยเชิงเส้น เท่ากับ y = 0.2296x - 0.0044 และมีค่าสัมประสิทธิ์สหสัมพันธ์ (R ) เท่ากับ 0.9994
ดังแสดงในภาพที่ 10 และตารางผนวกที่ 7 และสีของสารละลายมาตรฐานไนเตรทเข้มขึ้นตามค่าความ
เข้มข้นของสารละลายมาตรฐานที่เพิ่มขึ้นด้วย ดังแสดงในภาพที่ 11
สารละลายมาตรฐานไนเตรท
4
y = 0.2296x - 0.0044
ค่าการดูดกลืนแสง (Abs) 2
3
R² = 0.9994
1
0
0 2 4 6 8 10 12 14
ความเข้มข้นของสารละลายมาตรฐานไนเตรท (มิลลิกรัมต่อลิตร)
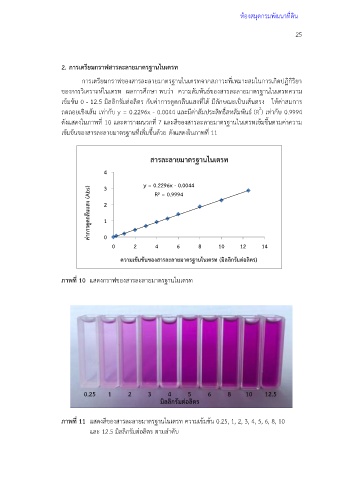
ภาพที่ 10 แสดงกราฟของสารละลายมาตรฐานไนเตรท
0.25 1 2 3 4 5 6 8 10 12.5
มิลลิกรัมต่อลิตร
ภาพที่ 11 แสดงสีของสารละลายมาตรฐานไนเตรท ความเข้มข้น 0.25, 1, 2, 3, 4, 5, 6, 8, 10
และ 12.5 มิลลิกรัมต่อลิตร ตามล าดับ